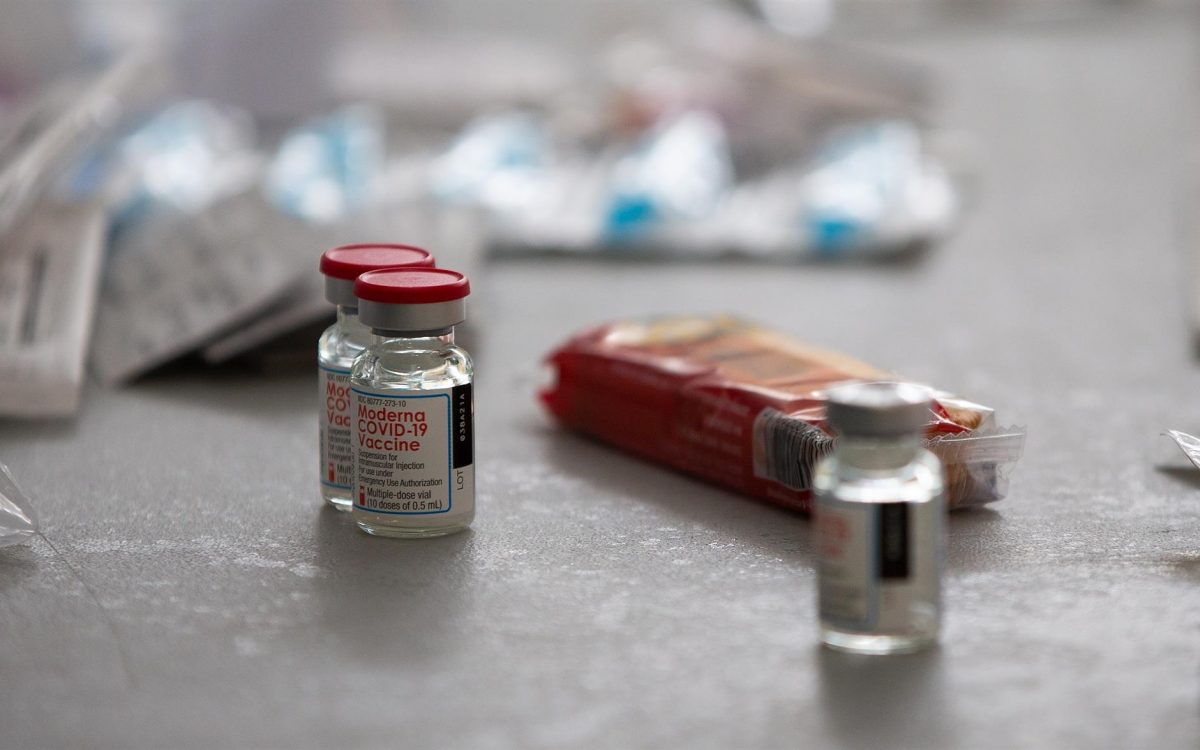
Foto: EFE/Cj Gunther/Archivo
(EFE).- Moderna anunció este martes que solicitó a los reguladores estadounidenses la aprobación plena de su vacuna contra la covid-19, que hasta ahora se usa bajo una autorización de emergencia.
De obtener esta licencia, la farmacéutica podría entre otras cosas vender dosis directamente a los consumidores y continuar comercializando la vacuna una vez que se declare el fin de la emergencia sanitaria.
La de Moderna es la segunda vacuna contra el coronavirus que busca la aprobación plena en EE.UU., después de que Pfizer y BioNTech presentasen su solicitud a comienzos de mayo.
La autorización completa requiere un proceso más estricto y la presentación de datos sobre la efectividad y seguridad de la vacuna durante al menos seis meses.
Tradicionalmente, los reguladores estadounidenses tardan un año o más en autorizar por esta vía medicamentos para el público general.
El consejero delegado de Moderna, Stéphane Bancel, se declaró en un comunicado satisfecho de dar “este importante paso en el proceso regulador en EE.UU.” y dijo que la empresa trabajará con la Administración Federal de Fármacos y Alimentos (FDA, en inglés) para presentar todos los datos requeridos.



